利用沉淀反应,可以进行某些离子间的分离。其中应用较多的是利用氢氧化物、硫化物沉淀进行分离。
(一)氢氧化物沉淀的分离
除碱金属和锶、钡的氢氧化物外,大多数金属氢氧化物都是难溶强电解质。由于难溶氢氧化物的溶度积有大有小,各不相同。因此,难溶氢氧化物开始沉淀和沉淀完全时的pH值范围不同,通过控制不同的pH值范围可以使不同的氢氧化物沉淀,以达到分离的目的。
【例7-8】某混合溶液中Cr3+和Cd2+的浓度都是0.010mol·L—1,若只要Cr3+沉淀,Cd2+不沉淀,从而达到分离的目的,问需控制pH值在什么范围?
{已知K■sp[Cr(OH)3]=6.3×10—31;K■sp[Cd(OH)2]=2.51×10—14}
解:若要Cr3+和Cd2+分离,必须使Cr3+沉淀完全,而Cd2+不沉淀留在溶液中,因此,只要计算出Cr(OH)3沉淀完全时的pH值和Cd(OH)2刚开始沉淀时的pH值即可控制。
Cr(OH)3沉淀完全时:
Cd(OH)2开始沉淀时:
因此,只要控制pH在5.60~8.20之间,即可使Cr3+和Cd2+分离。
实际工作中,溶液pH值的控制多采用缓冲溶液。
【例7-9】在10ml浓度均为0.20mol·L—1的Fe3+和Mg2+的混合液中,加入10ml0.20mol·L—1氨水,欲使Fe3+和Mg2+分离,最少应加入多少克NH4Cl。
{已知K■sp[Fe(OH)3]=4.0×10—38;K■sp[Mg(OH)2]=1.8×10—11}
解:混合后,溶液中各离子浓度为:
c(Fe3+)=0.10mol·L—1c(Mg2+)=0.10mol·L—1
c(NH3·H2O)=0.10mol·L—1
Fe3+沉淀完全时:
Mg2+开始沉淀时:
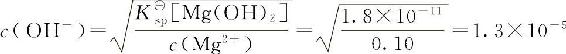
因此,控制1.3×10—5mol·L—1≥c(OH—)≥1.6×10—11mol·L—1,即可使Fe3+与Mg2+分离,由缓冲溶液计算c(OH—)公式:
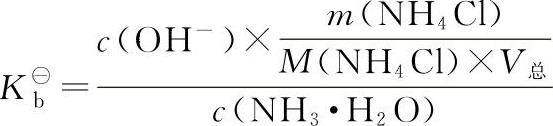
得:
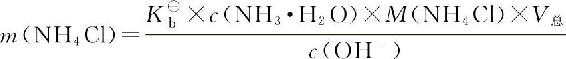
而要使Fe3+和Mg2+分离,
所以,至少加的NH4Cl质量为:
因此,至少要加入0.14gNH4Cl。
(二)硫化物的分离
由于难溶硫化物的K■sp大多相差较大,刚开始沉淀和沉淀完全时所需的S2—浓度不同,因此,可通过控制不同的pH范围,来控制不同的S2—浓度,从而使硫化物沉淀分离。
【例7-10】某溶液中含有Pb2+和Fe2+,二者浓度均为0.10mol·L—1,若利用通入H2S气体达饱和,使Pb2+和Fe2+分离,问溶液的pH值应控制在什么范围?[已知K■sp(PbS)=1.0×10—28;K■sp(FeS)=6.3×10—18]
解:由于两者的K■sp相差较大,因此,适当控制S2—浓度可使Pb2+沉淀完全,Fe2+不沉淀,即可使二者分离。
Pb2+沉淀完全时:
Fe2+开始沉淀时:
在饱和H2S溶液中,ceq(H2S)=0.10mol·L—1,溶液中的S2—浓度随H+浓度的变化而变化,关系式是:
将(1)式、(2)式中c(S2—)看作为ceq(S2—),分别代入(3)式得:
Pb2+沉淀完全时:

Fe2+开始沉淀时:
只要将pH控制在—0.49~2.92,即可使Pb2+和Fe2+分离。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















