3.1.3 三种典型的金属晶体结构
自然界中的晶体有成千上万种,它们的晶体结构各不相同,但若根据晶胞的三个晶格常数和三个轴间夹角的相互关系对所有的晶体进行分析,则发现可把它们的空间点阵分为14种类型。若进一步根据空间点阵的基本特点进行归纳整理,又可将14种空间点阵归属于7个晶系,如表3-1所示。
由于金属原子趋向于紧密排列,所以在工业上使用的金属元素中,除了少数具有复杂的晶体结构外,绝大多数都具有比较简单的晶体结构,其中最典型、最常见的金属晶体结构有3种类型,即体心立方晶格、面心立方晶格和密排六方晶格。前两者属于立方晶系,后者属于六方晶系。
表3-1 七种的晶系晶胞参数

1.体心立方晶格
体心立方晶格的晶胞如图3-2所示,为一个立方体。在立方体的八个顶角上各有一个与相邻晶胞共有的原子,立方体中心还有一个原子。晶格常数cba==,因此只用一个参数a表示即可。具有体心立方结构的金属有α–Fe、Cr、W、Mo、V、Nb、Ta等30多种。

图3-2 体心立方晶格示意图
(1)原子半径
晶胞中原子密度最大方向上相邻原子间距的一半尺寸称为原子半径。在体心立方晶格中,原子半径为体对角线(原子排列最密的方向)上原子间距的一半,即为 。
。
(2)原子数
一个晶胞内所包含的原子数目称为晶胞原子数。体心立方晶格中,由于立方体顶角上的原子为八个晶胞所共有,而立方体中心的原子为该晶胞所独有,因而晶胞原子数为 。
。
(3)配位数
所谓配位数是指晶体结构中与任一个原子最近邻且等距离的原子数目。显然,配位数越大,晶体中的原子排列便越紧密。体心立方晶胞中的任一原子(以立方体中心的原子为例)与八个原子接触且距离相等,因而体心立方晶格的配位数为8。
(4)致密度
若把原子看成刚性圆球,那么原子之间必然有间隙存在,原子排列的紧密程度可用原子所占体积与晶胞体积之比表示,称为致密度或密集系数,可用下式表示
![]()
式中 K——晶体的致密度;
n——一个晶胞实际包含的原子数;
V1——一个原子的体积;
V——晶胞的体积。
体心立方晶格的晶胞中含有两个原子,晶胞的棱边长度为a,原子半径为 ,其致密度为
,其致密度为
![]()
2.面心立方晶格
面心立方晶格的晶胞如图3-3所示。除在立方体的八个顶角上各有一个与相邻晶胞共有的原子外,在六个面的中心也各有一个共有的原子。γ–Fe、Ni、Al、Cu、Pb、Au、Ag等约有20种金属具有这种晶体结构。

图3-3 面心立方晶格的晶胞示意图
与体心立方晶格一样,晶格常数也是只用一个参数a表示。原子半径为面的对角线(原子排列最密的方向)上原子间距的一半,即 。由于立方体顶角上的原子为八个晶胞所共有,面上的原子为两个晶胞所共有,因而晶胞原子数为:
。由于立方体顶角上的原子为八个晶胞所共有,面上的原子为两个晶胞所共有,因而晶胞原子数为: 。面心立方晶格中每一个原子(以面的中心原子为例)在三维方向上各与四个原子接触且距离相等,因而配位数为12。其致密度为
。面心立方晶格中每一个原子(以面的中心原子为例)在三维方向上各与四个原子接触且距离相等,因而配位数为12。其致密度为
![]()
3.密排六方晶格
密排六方晶格的晶胞如图3-4所示,是一个正六棱柱体。在六棱柱的12个顶角及上下底面的中心各有一个与相邻晶胞共有的原子,两底面之间还有3个原子。具有密排六方结构的金属有Mg、Zn、Be、Cd等。
由图3-4可以看出,六棱柱顶角原子为六个晶胞共有,底面中心的原子为两个晶胞共有,两底面之间的三个原子为晶胞所独有,因而晶胞原子数为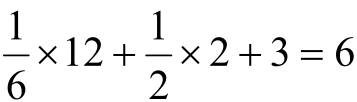 。密排六方晶格的晶格常数用六棱柱底面的边长a和高c表示,c与a之比c/a称为轴比。由于密排六方晶格中每一个原子(以底面中心的原子为例)与十二个原子(同底面上周围有六个,上下各三个)接触且距离相等,因而配位数为12,此时的轴比
。密排六方晶格的晶格常数用六棱柱底面的边长a和高c表示,c与a之比c/a称为轴比。由于密排六方晶格中每一个原子(以底面中心的原子为例)与十二个原子(同底面上周围有六个,上下各三个)接触且距离相等,因而配位数为12,此时的轴比 。对于典型的密排六方晶格金属,原子半径为底面边长的一半, 即r=a/2,致密度为:
。对于典型的密排六方晶格金属,原子半径为底面边长的一半, 即r=a/2,致密度为:


图3-4 密排六方晶格的晶胞示意图
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。

















