8.1 湿法刻蚀原理
在湿刻工艺中,应根据不同金属膜,选择不同的刻蚀药液。但是基本上都是利用强酸,如磷酸(H3PO4),硝酸(HNO3),盐酸(HCl),冰醋酸(CH3COOH)等及其混合物对金属的溶解和氧化还原过程,实现金属膜的图形化。
1.栅极湿刻(G-WE)反应机理
栅极一般由铝钕合金膜和钼铌合金膜组成,铝膜在下层,钼膜在上层。栅极膜层厚度为2 700左右,其中钼膜厚为700,铝膜厚为2 000。栅极刻蚀液要能够形成良好的铝和钼的刻蚀形状,与硅表面或绝缘膜表面不发生反应。栅极刻蚀液的成分和要求如表8.1和表8.2所示。
表8.1 栅极刻蚀液的组成混合比

表8.2 栅极刻蚀液的质量要求

硝酸使钼氧化成氧化钼(MoO3);磷酸用于铝及氧化钼的溶解;冰醋酸用于降低刻蚀液黏度以提高浸润性。
栅极刻蚀速度约为4 000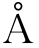 ·min-1。栅极刻蚀液是无色透明、有刺激性气味、强酸性液体,沾上皮肤会引起烧伤。因此作业时,应戴上耐酸性的手套、面罩并穿上前褂。具体的化学反应如下:
·min-1。栅极刻蚀液是无色透明、有刺激性气味、强酸性液体,沾上皮肤会引起烧伤。因此作业时,应戴上耐酸性的手套、面罩并穿上前褂。具体的化学反应如下:
Mo+2HNO3→MoO3+H2O+2NO2↑,
MoO3+H2O→H2MoO4(中间体),
12H2MoO4+H3PO4→H3[P(Mo3O10)4]+12H2O,
2Al+2H3PO4→2Al 3++2PO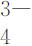 +3H2↑,
+3H2↑,
3H2+2HNO3→4H2O+2NO↑。
反应中要控制硝酸和冰醋酸的浓度。
2.漏极和源极湿刻(D-S-WE)反应机理
漏极和源极材料是金属铬,铬膜层厚度为1 400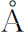 左右。漏极和源极刻蚀是一个氧化还原过程,刻蚀液的主要成分是硝酸铈铵(Ce(NH4)2(NO3)6)和硝酸。
左右。漏极和源极刻蚀是一个氧化还原过程,刻蚀液的主要成分是硝酸铈铵(Ce(NH4)2(NO3)6)和硝酸。
漏极和源极刻蚀液的组成混合比为:
Ce(NH4)2(NO3)6:14.0(1±0.5wt.%);
HNO3:10.0(1±0.5wt.%)。
硝酸铈铵的作用是与铬发生氧化还原反应,Ce4+把铬氧化成Cr6+,溶于刻蚀液中,而Ce4+离子被还原成Ce3+离子。硝酸的作用是防止铈的氢氧化物Ce(OH)3或Ce(OH)4的沉淀和析出。
D-S刻蚀速率大约为2 500·min-1。D-S刻蚀液是橙色,有刺激性气味的强酸性腐蚀液。Cr6+具有强氧化性,会造成皮肤溃烂。因此作业时,应戴上耐酸性的手套、面罩并穿上前褂。
具体的化学反应如下:
6Ce4++Cr →6Ce3++Cr6+,
Cr+2[Ce(NH4)2(NO3)6]→Cr2++2Ce3++2[(NH4)2(NO3)6]4-,
Cr+3[Ce(NH4)2(NO3)6]→Cr3++3Ce3++3[(NH4)2(NO3)6]4-。
总的化学方程式为
2Cr+12[Ce(NH4)2(NO3)6]+7H2O→
H2Cr2O7+12[Ce(NH4)2(NO3)5]+12HNO3。
反应中需要控制[Ce(NH4)2(NO3)6]的浓度。
3.像素电极的像素电极湿刻(PI-WE)反应机理
像素电极的主要成分为氧化铟(In2O3)和二氧化锡(SnO2),其中二氧化锡10%左右,是一种透明的导电膜,俗称ITO。膜厚度为400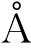 。刻蚀液的成分为盐酸、硝酸和去离子水的混合液。
。刻蚀液的成分为盐酸、硝酸和去离子水的混合液。
刻蚀液浓度配比一般为
HCl∶HNO3∶H2O=1∶0.08∶1(体积比);
HCl:17.6wt.%;
HNO3:1.6wt.%;
或者
HCl:18wt.%;
HNO3:3.2wt.%。
盐酸的作用是切断In—O、Sn—O的键,溶解In2O3和SnO2。
浓度为6mol·L-1的盐酸单体的刻蚀速度为190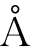 ·min-1。
·min-1。
浓度为6mol·L-1的硝酸单体的刻蚀速度为20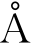 ·min-1。
·min-1。
硝酸作为一种氧化剂,加入后可以调节平衡状态并提高刻蚀速度。加入不同量的硝酸,刻蚀的速度有相当大的改变。在40℃的条件下,加入硝酸后刻蚀速度可以提高到174~260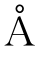 ·min-1。
·min-1。
但刻蚀速度过快会导致刻蚀的图形边缘劣化,如基板通过液切风刀时,由于搬送速度较慢,基板上药液流量的差异,因此会使图案产生较大的差别。
加入硝酸还可以软化光刻胶,提高光刻胶与膜层之间的渗透性,有利于提高ITO的刻蚀形状。
像素电极的刻蚀液是一种无色透明、有刺激性气味的腐蚀性酸性液体。因此作业时,应戴上耐酸性的手套、面罩并穿上前褂。
具体的化学反应如下:
In2O3+6HCl→2In3++6Cl-+3H2O,
SnO2+4HCl →Sn4++4Cl-+2H2O,
HNO3幑幐H++NO3-,
H++Cl-幑幐HCl。
在刻蚀过程中,Cl-浓度和NO-3浓度不发生变化,不需要对浓度进行特别控制。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














