第六节 镀铅锡合金溶液
一、氟硼酸镀铅锡合金溶液
分析成分:铅、锡、游离氟硼酸、游离硼酸、对苯二酚。
1.铅的测定
(1)试剂。
①3%过氧化氢溶液。
②20%三乙醇胺。
③缓冲溶液(pH为10)。
④铬黑T指示剂。
⑤0.05mol/L硫酸锌标准溶液。
⑥0.05mol/LEDTA标准溶液。
(2)分析方法。
在酸性溶液中,铅、锡与EDTA均能络合。在pH为10的情况下,用三乙醇胺使锡—EDTA解络而析出EDTA,以铬黑T为指示剂,用锌标准溶液进行返滴定的。根据EDTA和锌溶液的用量,可以求出铅的含量。
用移液管吸取镀液2mL置于250mL锥形瓶中,加H2O2数滴,准确加0.05mol/LEDTA标准溶液25mL,加水100mL,加20%三乙醇胺2.5mL,加缓冲溶液(pH为10)10mL及铬黑T指示剂数滴,用0.05mol/L硫酸锌标准溶液返滴定至由蓝色变红色为终点。
(3)计算。
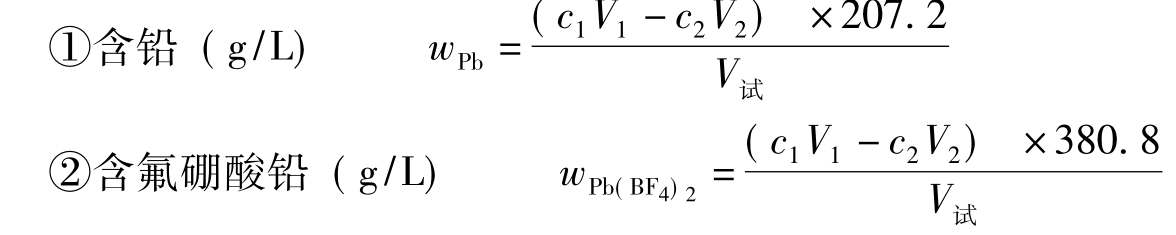
式中c1为EDTA标准溶液的浓度;V1为耗用EDTA标准溶液的体积;c2为硫酸锌标准溶液的浓度;V2为耗用硫酸锌标准溶液的体积;V试为试样的体积(mL);207.2为MPb;350.8为MPb(BF4)2。
2.二价锡的测定
(1)试剂。
①20%硫酸溶液。
②1%淀粉溶液。
③0.1mol/L碘标准溶液。
(2)分析方法。
铅锡合金镀液中主要含有铅、锡金属离子,它们基本上以二价状态存在。先用硫酸使二价铅生成硫酸铅沉淀,再以淀粉为指示剂,用碘标准溶液滴定二价锡。用移液管吸取镀液5mL置于250mL锥形瓶中,加水100mL,加20%硫酸20mL,充分搅拌,静置使沉淀下沉,再滴加硫酸,检查二价铅是否沉淀完全。加1%淀粉溶液2mL,用0.1mol/L碘标准溶液滴定至蓝色不消失为终点。
(3)计算。

式中c为碘标准溶液的浓度;V为耗用碘标准溶液的体积(mL);V试为试样的体积(mL);118.7为MSn;292为
MSn(BF4)2。
(4)附注。
总锡按碱性镀锡溶液碘量法测定,从中减去Sn2+量,可得Sn4+量。
3.锡、铅的连续测定
(1)试剂。
①醋酸缓冲溶液(pH为5.5)。称醋酸铵136g溶于水中,加醋酸15mL,稀释至1L并用醋酸调至pH为5.5。
②二甲酚橙指示剂。
③氟化铵,固体。
④0.05mol/LEDTA标准溶液。
⑤0.05mol/L铅标准溶液。
(2)分析方法。
铅锡合金镀液中主要含有铅、锡金属离子,它们在酸性溶液中能与EDTA生成稳定的络合物(pH为4~5),但锡与EDTA的络合物能被氟化铵置换而析出EDTA。因此,可以在醋酸缓冲溶液中,以二甲酚橙为指示剂,用铅标准溶液滴定析出的EDTA,从总量中减去锡量,求得铅量。
用移液管吸取镀液2mL置于300mL锥形瓶中,加水100mL,加醋酸缓冲溶液15mL,准确加入0.05mol/LEDTA标准溶液25mL(V),加二甲酚橙指示剂3~5滴,用0.05mol/L铅标准溶液滴定至由黄色变红色为终点。记录耗用量为V1(mL)。然后加入氟化铵2~3g,稍加热或放置15min,溶液变为黄色,再用0.05mol/L铅标准溶液滴定至由黄色变红色,此时可补加少许氟化铵,摇动并微热,溶液若再变为黄色,冷却后继续滴定,使溶液再变红色。记录耗用量为V2(mL)。经补加氟化铵和加热,溶液不再变黄色时,证明滴定已达终点。
(3)计算。
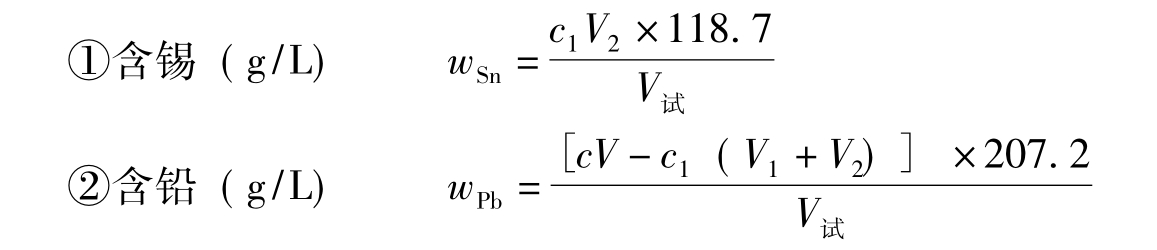
式中c为EDTA标准溶液的浓度;V为耗用EDTA标准溶液的体积(mL);c1为铅标准溶液的浓度;V1为第一次滴定耗用铅标准溶液的体积(mL);V2为第二次滴定耗用铅标准溶液的体积(mL);V试为试样的体积(mL);118.7为MSn;207.2为MPb。
4.游离氟硼酸的测定
(1)试剂。
①30%硫酸钠溶液。
②亚甲基蓝—甲基磺混合指示剂1份0.1%亚甲基蓝乙醇溶液与1份0.1%甲基磺乙醇溶液相混合。
③1mol/L氢氧化钠溶液。
(2)分析方法。
采用中和法,以亚甲基蓝—甲基磺混合为指示剂,用氢氧化钠滴定,溶液由蓝紫色变成绿色为终点。吸取镀液5mL于250mL锥形瓶中,加10mL硫酸钠溶液,50mL水,再加入10滴混合指示剂,用1mol/L氢氧化钠滴定至溶液由蓝紫变为绿色为终点。
(3)计算。
![]()
式中c为氢氧化钠标准溶液浓度;V为消耗氢氧化钠标准溶液体积(mL);87.83为MHBF4。
5.对苯二酚的测定
(1)试剂。
①15%硫酸钠溶液。
②甘油(1+1)或甘露醇(固体)。
③酚酞指示剂。
④硫酸1+1。
⑤邻菲罗啉—亚铁指示剂称取1.624g盐酸邻菲罗啉及0.6959g硫酸亚铁溶于100mL水中,混匀。
⑥1mol/L氢氧化钠标准溶液。
⑦0.1mol/L硝酸铈铵标准溶液。称取已在120℃烘干的硝酸铈铵55g,用每升含有30g硫酸的溶液溶解并稀释至1L,以邻菲罗啉为指示剂,用0.1mol/L硫酸亚铁铵标准溶液进行标定。
(2)分析方法。
先用硫酸钠将二价铅沉淀为硫酸铅,再加入甘油或甘露醇,以酚酞为指示剂,用氢氧化钠标准溶液滴定二价锡及硼酸。过滤,在滤液中以邻菲罗啉为指示剂,用硝酸铈铵标准溶液氧化对苯二酚为对苯醌。稍过量的铈与指示剂中硫酸亚铁作用,由橙红色变淡蓝色为终点。
C6H4(OH)2+2Ce(NO3)4─→C6H4O2+2Ce(NO3)3+2HNO3
用移液管吸取镀液10mL置于300mL烧杯中,加水30mL、15%硫酸钠溶液10mL及甘油20mL,用玻璃棒充分搅拌,加酚酞指示剂数滴,用1mol/L氢氧化钠标准溶液滴定至粉红色。将溶液和沉淀一起移入250mL容量瓶中,以水稀释至刻度,摇匀。用干滤纸过滤后,以移液管吸取滤液50mL,置于250mL锥形瓶中,加1+1硫酸10~15mL及邻菲罗啉—亚铁指示剂5~8滴,用0.1mol/L硝酸铈铵标准溶液滴定至溶液由橙红色变淡蓝色为终点。
(3)计算。
式中c为硝酸铈铵标准溶液的浓度;V为耗用硝酸铈铵标准溶液的体积(mL);V试为试样的体积(mL);110.12为MC6H4(OH)2。
(4)附注。
正常情况下,终点突变明显,重现性较好。若出现终点不明显,可补加2~5mL1+1硫酸溶液。
二、柠檬酸镀铅锡合金溶液
1.柠檬酸的测定
(1)试剂。
①硫酸,20%,1+4,5%。
②碘化钾,固体。
③硫酸锰,固体。
④淀粉指示剂。
⑤0.02mol/L高锰酸钾标准溶液。
⑥0.1mol/L硫代硫酸钠标准溶液。
(2)分析方法。
在酸性溶液中,高锰酸钾将柠檬酸氧化反应完成后,加入碘化钾,使剩余的高价锰和碘化钾反应生成游离碘,用硫代硫酸钠标准溶液滴定游离碘,以此计算柠檬酸的含量。
吸取5mL镀液于400mL烧杯中,加水100mL,20%硫酸20mL,放置半小时,将沉淀用已知质量的玻璃砂芯漏斗过滤,用5%硫酸洗4次,水洗4次。在滤液中,加水50mL,加1+4硫酸10mL及硫酸锰1g,加热至70℃,在不断搅拌下,缓缓加入0.02mol/L高锰酸钾标准溶液25mL,在温热处(约70℃)放置5min,用流水冷却,加碘化钾固体2g,摇匀,用硫代硫酸钠标准溶液滴定至淡黄色,加淀粉3mL,继续滴定至蓝色消失为终点(V)。
①K值求法。吸取0.02mol/L高锰酸钾标准溶液25mL于250mL锥形瓶中,加水150mL,1+4硫酸10mL,硫酸锰(MnSO4)1g,加碘化钾(固体)2g,摇匀,用0.1mol/L硫代硫酸钠标准溶液滴定至淡黄色。加淀粉3mL,继续滴定至蓝色消失为终点(V1)。
![]()
K为0.1mol/L硫代硫酸钠标准溶液相当的高锰酸钾体积(mL)。
②滴定度(T)求法。先配制一已知含量的柠檬酸的镀液(设含柠檬酸为w,单位为g/L),吸取10mL,按上法操作,加入0.02mol/L高锰酸钾25mL,0.01mol/L硫代硫酸钠标准溶液V2(mL),则
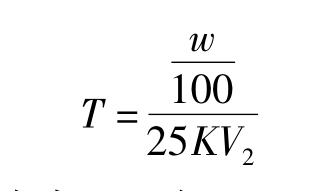
式中T为1mL0.02mol/L高锰酸钾标准溶液相当柠檬酸的质量(g)。
(3)计算。
![]()
式中V试为所取体积(mL);V为试液所耗0.1mol/L硫代硫酸钠标准溶液体积(mL)。
2.铅、锡的连续测定
(1)试剂。
①醋酸缓冲溶液(pH为5.5)。
②二甲酚橙指示剂。
③氟化氨,固体。
④0.05mol/LEDTA标准溶液。
⑤0.05mol/L铅标准溶液。
(2)分析方法。
铅锡金属离子,它们在酸性溶液中能与EDTA生成稳定络合物(pH为4~5),但锡与EDTA络合物能被氟化物置换而析出EDTA。因此,可以在醋酸缓冲溶液中,以二甲酚橙为指示剂,用标准铅溶液滴定析出的EDTA,用总量减去锡量,求得铅量。
吸取镀液2mL于250mL锥形瓶中,加水100mL,加醋酸缓冲溶液1mL,准确加入0.05mol/LEDTA标准溶液25mL(V),加二甲酚橙指示剂2滴,用0.05mol/L铅标准溶液滴定至黄色变为红色为终点。记录耗用量为V1(mL)。然后加入氟化铵1g,摇动并微热,溶液若再变为黄色,冷却后继续滴定,使溶液再变红色,记录耗用量为V2(不包括V1),再补加氟化铵和加热,直到溶液不再变黄色时证明滴定已到终点。
(3)计算。
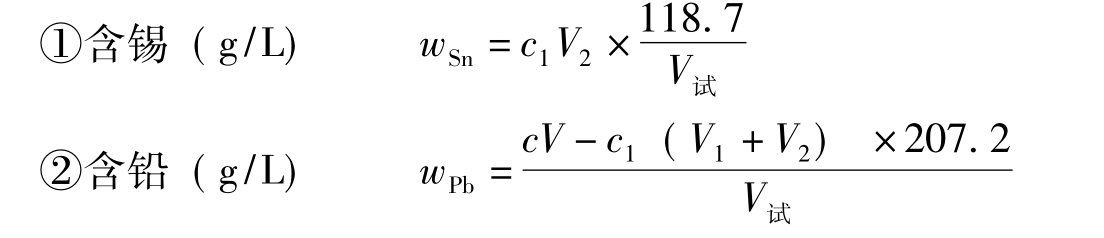
式中c为EDTA标准溶液的浓度;V为耗用EDTA标准溶液的
体积(mL);c1为铅标准溶液的浓度;V1为第一次滴定耗用铅标准溶液的体积(mL);V2为第二次滴定耗用铅标准溶液的体积(mL);V试为试样体积(mL);118.7为MSn;207.2为MPb。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。

















