2.1.7 平均碰撞频率和平均自由程
在气体中,大量分子作永不停息的无规则热运动,彼此之间会不断发生碰撞。就单个分子来说,与其他分子的碰撞在时间和空间上都是随机的。但对大量分子来说,分子间的碰撞服从确定的统计规律。
1.分子的平均碰撞频率
一个分子在单位时间内与其他分子碰撞的平均次数,称为分子的平均碰撞频率,用-Z表示。从理论上可导出
![]()
式中:d为分子的有效直径,这里假设分子是直径为d的小球,d的数量级约为10-10m;n如前
所述为分子数密度;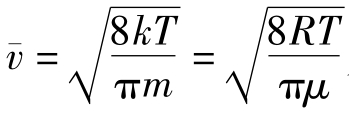 为分子的平均速率,公式来源详见下面有关麦克斯韦速率分布律的讨论。
为分子的平均速率,公式来源详见下面有关麦克斯韦速率分布律的讨论。
由此可知,分子数密度n越大,温度T越高,分子之间的碰撞就越频繁,平均碰撞频率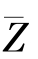 值越大。
值越大。
2.分子的平均自由程
一个分子在相邻的两次碰撞之间所飞行的直线距离称为自由程。由于碰撞是随机的,单个分子的自由程也是随机的。然而,大量分子的自由程却具有确定的统计规律性。自由程的统计平均值称为平均自由程,用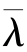 表示。由于单位时间内气体分子运动的平均路程为
表示。由于单位时间内气体分子运动的平均路程为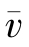 ,在此期间与其他分子的碰撞次数为
,在此期间与其他分子的碰撞次数为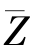 ,所以分子的平均自由程为
,所以分子的平均自由程为
![]()
此式说明,对一定的气体而言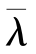 与分子数密度n成反比,而与平均速率
与分子数密度n成反比,而与平均速率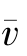 无关。
无关。
根据p=nkT,分子的平均自由程还可以表示为
![]()
这表明,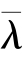
和温度与压强的比值T/p成正比关系。
在标准状态下,氢气分子的平均碰撞频率数量级约为109s-1,平均自由程数量级约为10-7m。
【例2.1-4】一定量的理想气体,经等压过程从体积V0膨胀到2V0,其平均自由程由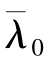 变为
变为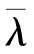 ,平均碰撞频率由
,平均碰撞频率由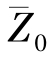 变为
变为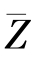 ,则正确结果是( )。
,则正确结果是( )。
![]()
解:平均自由程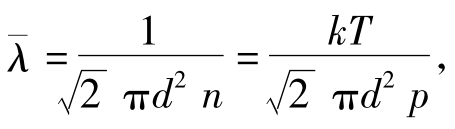 对等压过程,V∝T,体积加倍V0→2V0,温度也加倍T0→2T0,所以有
对等压过程,V∝T,体积加倍V0→2V0,温度也加倍T0→2T0,所以有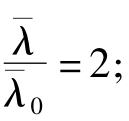 平均碰撞频率
平均碰撞频率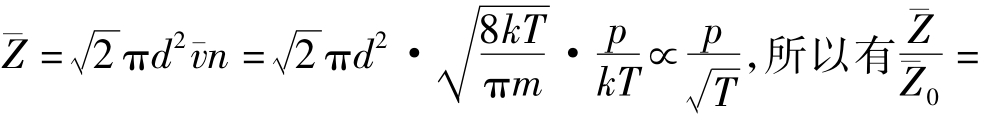
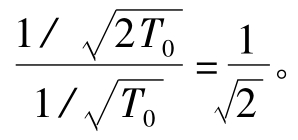 正确答案为(C)。
正确答案为(C)。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。

















