实验82 固体超强酸的制备及乙酸正丁酯的合成与表征
实验目的
了解固体酸催化剂的一般制备方法和在有机合成中的应用;巩固晶体结构、酯化反应、高温固相合成等知识及化学实验单元操作的基本技能;学习气相色谱,巩固X射线粉末衍射等近代测试仪器的使用方法;加强环保意识,认识绿色化学合成手段在化工生产中应用的重要性与必要性。
实验原理
ZrO2分别经过硫酸、钼酸铵溶液浸泡,于400~700℃下灼烧,得到具有较高活性的固体超强酸催化剂。在丁醇和乙酸的酯化反应中,用制备的催化剂代替浓硫酸来催化反应。酯化反应结束后,产物乙酸正丁酯经蒸馏与反应系统分离,产物纯度高,没有废液排放,催化剂可反复使用。
产物经103型气相色谱仪进行色谱分析(关于氢火焰色谱分析的操作参考有关色谱分析书籍),鉴定产物纯度,计算产率。
实验用品
仪器 烧杯(100mL);圆底烧瓶(100mL);水分离器(10mL);蒸馏头;球形冷凝器;直形冷凝器;接收管;锥形瓶(50mL);布氏漏斗;抽滤瓶;量筒(50mL,10mL);电热套或煤气灯;坩埚;台秤;103型气相色谱仪(公用)等。
试剂 ZrO2(s);冰醋酸;丁醇;硫酸(1mol·L-1);钼酸铵(0.5mol·L-1)等。ZrO2为工业品,其余均为分析纯试剂。
实验步骤
1.固体超强酸催化剂的制备
用台秤称取5g ZrO2·nH2O,倾入装有75mL 1mol·L-1 H2SO4溶液的100mL烧杯中,浸泡24h。真空过滤,滤液倒入废酸回收容器内,滤饼再用10mL 0.5mol·L-1钼酸铵溶液浸泡24h,真空过滤,滤液倒入专用回收瓶,滤饼置于烘箱中,110℃烘2h,再置于马弗炉内600℃灼烧3h,待马弗炉自然冷却后取出,粉碎,备用(请自学产物的鉴定知识)。
2.乙酸正丁酯的制备
在装有电热套(或用煤气灯加热)的100mL圆底烧瓶中,加入1g上述制备好的催化剂,25mL正丁醇,14.3mL冰醋酸,几粒沸石,装上水分离器及球形回流冷凝器,开启冷却水。当烧瓶内液体沸腾,冷凝器有回流液滴下时,调节热源,使回流速度正常。1h后,在水分离器中可以看到反应生成的水出现。待基本没有水滴下时(需3~4h),将仪器由回流装置改为简单蒸馏装置,收集124~126℃馏分,用作气相色谱分析。低沸点馏分及残液倒入回收瓶,固体催化剂可循环使用。
3.产品的气相色谱分析
用103型气相色谱仪,氢火焰离子化检测器对产品进行分析,具体操作条件如下。
进样器温度:180℃ 载气流量(N2):35mL·min-1
氢火焰检测器温度:140℃空气流量:250mL·min-1
柱箱温度:60℃氢气流量:110mL·min-1
衰减:1/4灵敏度:106
记录仪走纸速度:4mm·min-1进样量:0.6μL
记录仪量程:1mV
纯乙酸正丁酯为无色液体,沸点为126.5℃,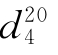 为0.8825,
为0.8825,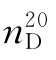 为1.3941。乙酸正丁酯的红外光谱如图5-43所示。
为1.3941。乙酸正丁酯的红外光谱如图5-43所示。
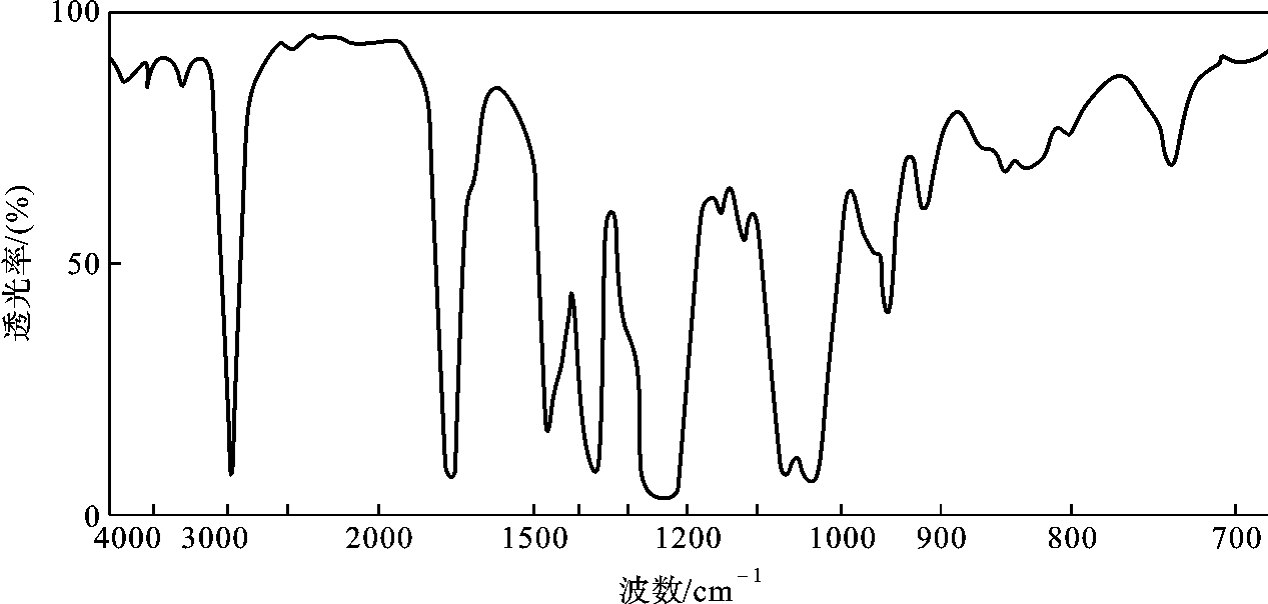
图5-43 乙酸正丁酯的红外光谱图
思考题
比较固体超强酸和浓硫酸催化剂催化酯化反应的优缺点。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















