实验五 总氮的测定与分析
一、实验目的和要求
在生物脱氮工艺中,氮的脱除是通过硝酸盐还原为氮气并从废水中排出实现的,通过测定总氮可以了解生物脱氮效果的好坏。以下规定了用碱性过硫酸钾在120~124℃消解,紫外分光光度测定水中总氮的方法。
二、实验原理
在60℃水溶液中,过硫酸钾可分解产生硫酸氢钾和原子态氧,硫酸氢钾在溶液中离解而产生氢离子,故在氢氧化钠的碱性介质中可促使分解过程趋于完全。
分解出的原子态氧在120~124℃条件下,可使水样中含氮化合物的氮元素转化为硝酸盐。并且在此过程中有机物同时被氧化分解。可用紫外分光光度法于波长220nm和275nm处,分别测出吸光度A220及A275按式①求出校正吸光度A:
![]()
三、适用范围
本方法适用于地面水、地下水的测定,可测定水中亚硝酸盐氮、硝酸盐氮、无机铵盐、溶解态氨及大部分有机含氮化合物中氮的总和。
氮的最低检出浓度为0.050mg/L,测定上限为4mg/L。
本方法的摩尔吸光系数为1.47×103 L/(mol·cm)。
测定中干扰物主要是碘离子与溴离子,碘离子相对于总氮含量的2.2倍以上,溴离子相对于总氮含量的3.4倍以上有干扰。
四、定义
(1)可滤性总氮 指水中可溶性及含可滤固体(小于0.45μm颗粒物)的含氮量。
(2)总氮 指可溶性及悬浮颗粒中的含氮量。
五、试剂和材料
除非另有说明,分析时均使用符合国家标准或专业标准的分析纯试剂。
(1)水,无氨
按下述方法之一制备。
①离子交换法。将蒸馏水通过一个强酸型阳离子交换树脂(氢型柱),流出液收集在带有密封玻璃盖的玻璃瓶中。
②蒸馏法。在1 000mL蒸馏水中,加入0.10mL硫酸(ρ=1.84g/mL)。并在全玻璃蒸馏器中重蒸馏,弃去前50mL馏出液,然后将馏出液收集在带有玻璃塞的玻璃瓶中。
(2)氢氧化钠溶液(200g/L):称取20g氢氧化钠(NaOH),溶于水中,稀释至100mL。
(3)氢氧化钠溶液(20g/L):将上一步的溶液稀释10倍而得。
(4)碱性过硫化钾溶液:称取40g过硫化钾(K2S2O4);另称取15g氢氧化钠(NaOH),溶于水中,稀释至1 000mL,溶液存放在聚乙烯瓶内,最长可储存一周。
(5)盐酸溶液:1∶9(体积比)。
(6)硝酸钾标准溶液。
①硝酸钾标准储备液,cN=100mg/L,硝酸钾(KNO3)在105~110℃烘箱中干燥3h,在干燥器中冷却后,称取0.721 8g,溶于水中,移至100mL容量瓶中,用水稀释至标线在0~10℃暗处保存,或加入1~2mL三氯甲烷保存,可稳定6个月。
②硝酸钾标准使用液,cN=100mg/L:将储备液用水稀释10倍而得。使用时配制。
(7)硫酸溶液,1∶35(体积比)。
六、仪器和设备
(1)常用实验仪器和下列仪器。
(2)紫外分光光度计及10mm石英比色皿。
(3)医用手提式蒸汽灭菌器或家用压力锅,锅内温度相当于120~124℃。
(4)具玻璃磨口塞比色管,25mL。
所有玻璃器皿可以用盐酸(1∶9)或硫酸(1∶35)浸泡,清洗后再用水冲洗数次。
七、样品
1.采样
在水样采集后立即放入冰箱中或低于4℃的条件下保存,但不得超过24h。水样放置时间较长时,可在1 000mL水样中加入约0.5mL硫酸(ρ=1.84g/mL),酸化到pH小于2,并尽快测定。
样品可储存在玻璃瓶中。
2.试样的制备
取实验室样品用氢氧化钠溶液或硫酸溶液调节pH至5~9从而制得试样。
八、分析步骤
1.测定
(1)用无分度吸管取10.00mL试样(cN超过100μg时,可减少取样量并加水稀释至10mL)置于比色管中。
(2)试样不含悬浮物时,按下述步骤进行。
①加入5mL碱性过硫酸钾溶液,塞紧磨口塞用布及绳等方法扎紧瓶塞,以防弹出。
②将比色管置于医用手提蒸汽灭菌器中,加热,使压力表指针到1.1~1.4kg/cm2,此时温度达120~124℃后开始计时。或将比色管置于家用压力锅中,加热至顶压阀吹气时开始计时。保持此温度加热0.5h。
③冷却,开阀放气,移去外盖,取出比色管并冷至温室。
④加盐酸(1∶9)1mL,用无氨水稀释至25mL标线,混匀。
⑤移取部分溶液至10mm石英比色皿中,在紫外分光光度计上,以无氨水作参比,分别在波长为220nm与275nm处测定吸光度,并用式①计算出校正吸光度A。
(3)试样含悬浮物时,先按上述步骤①至④进行,然后待澄清后移取上清液到石英比色皿中。再按上述步骤⑤进行。
2.空白实验
空白实验除以10mL水代替试样外,采用与测定完全相同的试剂、用量和分析步骤进行平行操作。
[注] 当测定在接近检测限时,必须控制空白实验的吸光度Ab不超过0.03;超过此值,要检查所有水、试剂、器皿和家用压力锅或医用手提灭菌器的压力。
3.校准
(1)校准系列的准备
①用分度吸管向一组(10支)比色管中,分别加入硝酸盐氮标准使用溶液0.0mL,0.10mL,0.30mL,0.50mL,0.70mL,1.00mL,3.00mL,5.00mL,7.00mL,10.00mL。加水稀释至10.00mL。
②按分析步骤①~④进行测定。
(2)校准曲线的绘制
零浓度(空白)溶液和其他硝酸钾标准使用溶液制得的标准系列完成全部分析步骤,于波长220nm和275nm处测定吸光度后,分别按下式求出除零浓度外其他校准系列的校正吸光度As和零浓度的校正吸光值Ab及其差值At

按At值与相应的NO3-N含量(μg)绘制标准曲线。
九、结果的表示
1.计算方法
按式①计算得试样校正吸光度At,在校准曲线上查出相应的总氮μg数,总氮含量cN(mg/L)按下式计算:
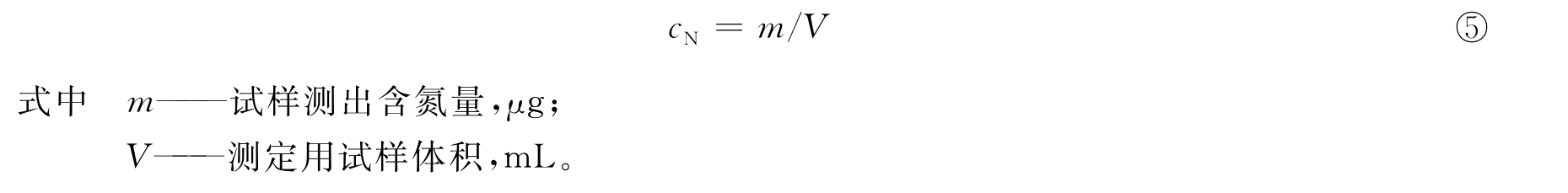
2.重复性
21个实验室分别测定了亚硝酸盐,氨基丙酸与氯化铵的混合样品;CW604氨氮标准样品;L-谷氨酸与葡萄糖混合样品。上述三种样品分别为1.49mg/L,2.64mg/L,1.15mg/L,其结果如下:各实验室的室内相对标准差分别为2.3%,1.6%,2.5%。室内重复测定允许精密度分别为0.074mg/L,0.092mg/L和0.063mg/L。
3.再现性
各实验室对上述三种统一合成样品测定,实验室间相对标准偏差分别为3.1%,1.1%和4.9%。
4.准确度
各实验室对上述三种统一合成样品测定,实验室内均值相对误差分别为6.3%,2.4%和8.7%。
室内重复测定相对误差分别为7.5%,3.8%和9.8%。实验室平均回收率置信范围分别为(99.0±6.4)%,(99.0±5.1)%和(101±9.4)%。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














